必看!20项细胞治疗项目获批!1.6 万元/次起(附:价格清单)
引言
2026年3月22日,第三届博鳌乐城干细胞大会上传来重磅消息,海南博鳌乐城先行区正式公布新一批可收费细胞治疗项目(新增6项)。
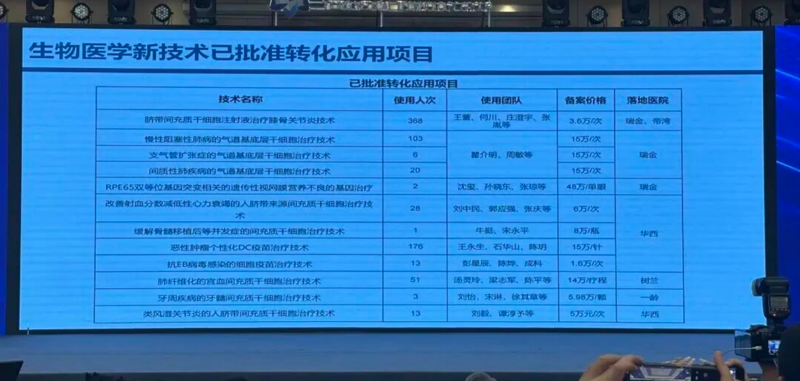
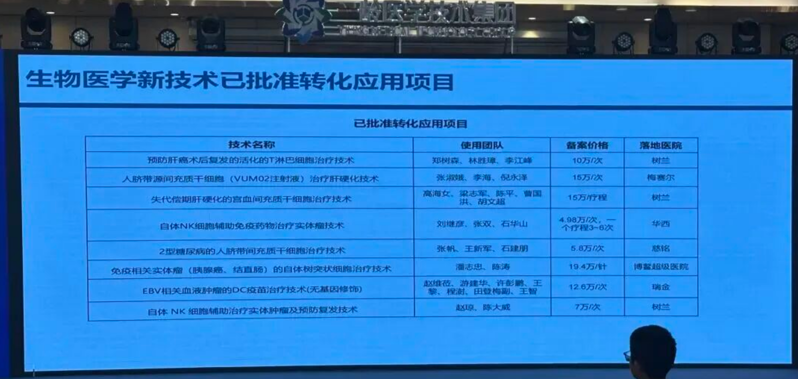
叠加之前获批的合规项目,博鳌乐城已累计批准20项生物医学新技术转化应用项目,这些项目不仅价格透明、落地医院明确、适应症清晰,更构建了可复制、可推广的临床转化模式,为全国细胞治疗产业发展提供了宝贵经验。
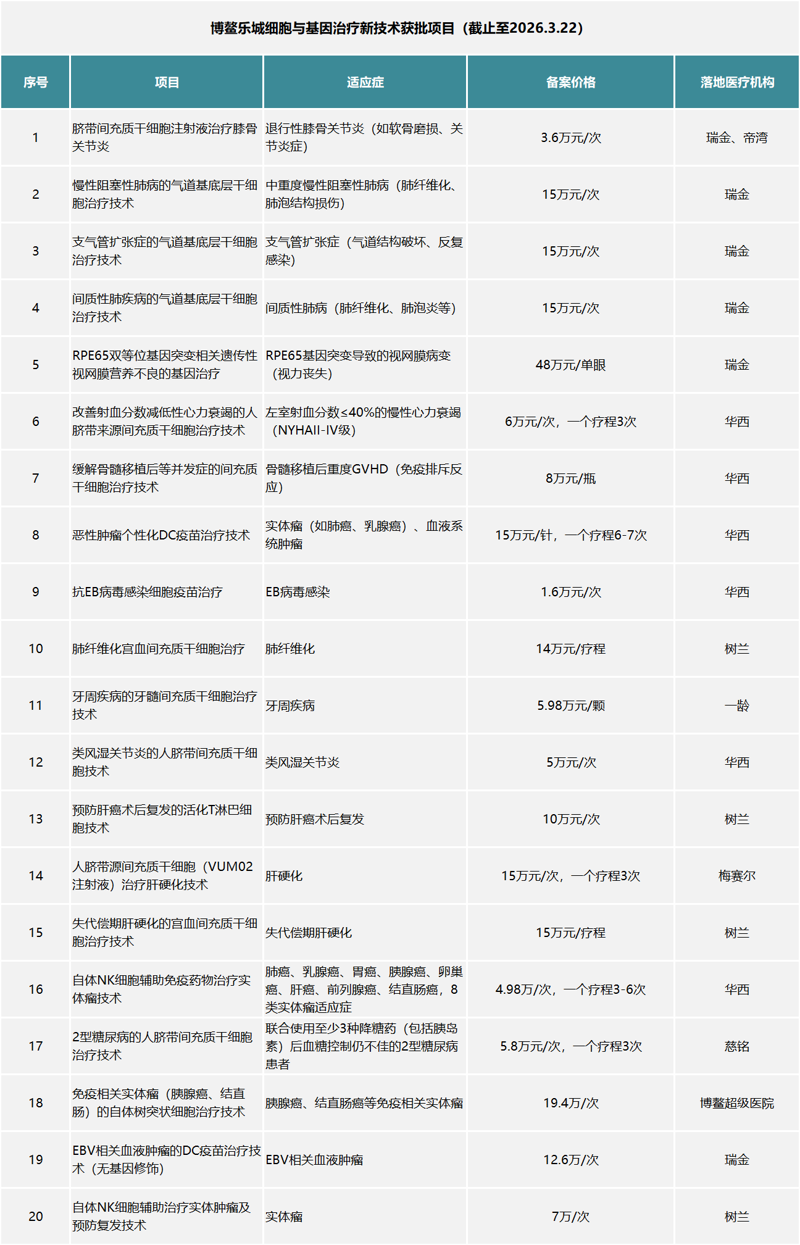
生物医学新技术临床转化应用日渐成熟
如今,细胞治疗已从实验室探索稳步迈向临床应用阶段,成为攻克疑难疾病、补充传统治疗手段的重要方向,临床转化应用成熟度持续提升,为更多患者带来了新的治疗希望。
随着《生物医学新技术临床研究和临床转化应用管理条例》(国务院第818号令)的即将施行(2026年5月1日),药品监管与医疗技术管理的“双轨制”将在全国层面正式落地施行,为细胞治疗临床转化划定了清晰的合规路径。
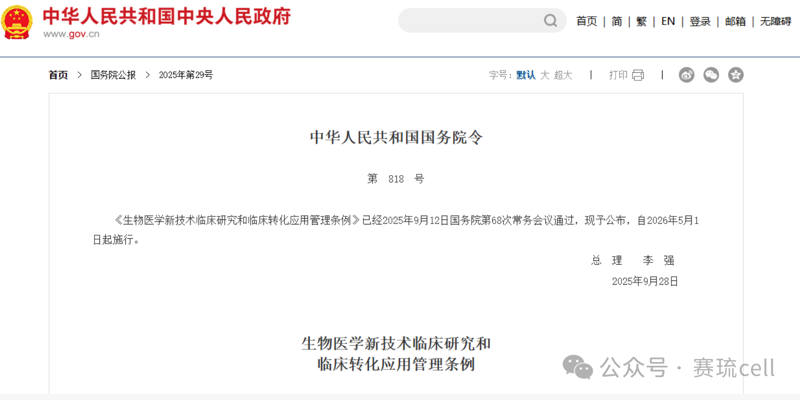
这其中,“医院+企业”的协同合作模式,成为当前细胞治疗实现临床转化、坚守合规发展的核心路径。
根据818号令相关要求,仅三级甲等医院具备开展生物医学新技术临床研究的资质,企业需与三甲医院签订规范的书面协议,明确双方职责、研究方案、数据所有权及收益分配等核心内容,通过IIT(研究者发起的临床试验)备案、NMPA药品注册、配套服务支持等合规路径,实现技术的临床转化与收益的合法兑现。
锐赛生物:院企协同 共促产业高质量发展
此次海南博鳌乐城获批的20项细胞治疗项目中,多项DC细胞相关技术成功入选,涵盖免疫相关实体瘤、EBV相关血液肿瘤等多个适应症,这也印证了DC细胞治疗技术的临床价值与市场潜力。
在DC细胞领域,锐赛生物已深耕多年,凭借深厚的技术积淀与成熟的临床合作体系,早早布局合规发展,与上海、浙江等多地多家三甲医院建立紧密合作关系,联合开展了十数项DC细胞相关的IIT项目,积累了丰富的临床研究经验与技术成果。

在818号令的合规要求下,未来锐赛生物将进一步强化与各大三甲医院的协同合作,严格遵循临床研究备案、伦理审查等各项规定,规范协议流程、规避合规风险。
同时,充分发挥自身在细胞技术研发、细胞制备与质控、基因检测等方面的核心优势,为合作医院提供专业、高效的配套支持,推动生物医学新技术的合规转化与临床落地,最终实现院企双赢,为细胞治疗产业的高质量发展注入新动能,让更多患者受益于前沿生物医学技术的进步。
内容来源网络公开资料,锐赛新媒体中心 综合整理。
声明:本文内容仅用于科普交流,不构成任何医疗建议或治疗方案推荐。
文中涉及的科研成果、临床数据等信息均来源于公开文献及权威机构发布,仅供参考。由于医学的复杂性,个体案例不代表普遍疗效,请勿盲目解读。
本平台不对用户基于本文内容作出的任何决策承担责任,相关治疗请务必前往正规医疗机构,在专业医生指导下进行。
本文图片来源网络,如有版权问题请联系删除。本声明最终解释权归公众号所有。


