护端粒!抗衰老!围产组织来源干细胞为啥更能打?
引言
随着年龄的增长,我们的身体逐渐进衰老,器官功能渐退、免疫力悄悄下降,各种与年龄相关的健康问题随之浮现。而在这一系列变化背后,藏着一个关键的 “衰老密码”:端粒的缩短。
端粒:细胞衰老的 “生命时钟”
端粒,是染色体末端的 “保护帽”,就像鞋带末端的塑料头,守护着遗传物质的稳定。但这个 “保护帽” 并非永恒 —— 每次细胞分裂复制,端粒都会不可避免地缩短一截。
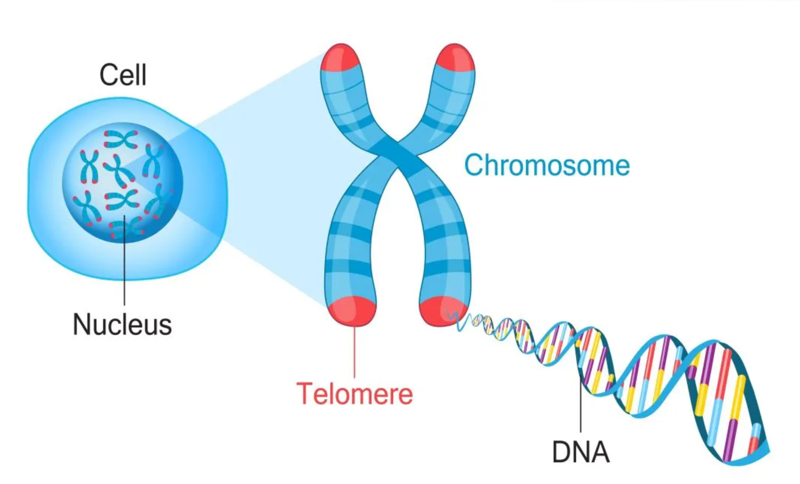
当它短到临界值,细胞就会进入 “衰老状态”:停止分裂、失去再生能力,机体的自我修复系统也随之 “失灵”。更让人在意的是,若端粒因环境污染、精神压力等内外应激因素提前受损,衰老进程还会被 “加速推进”。
那么,如何才能抵抗端粒的缩短?
一篇发表于《Bioengineering》的最新综述探讨了间充质干细胞(MSCs)及其衍生的细胞外囊泡(EVs,主要是外泌体)在预防端粒缩短、细胞衰老和加速生物衰老中的作用机制和潜在应用价值。

干细胞及外泌体:对抗端粒缩短 “新势力”
端粒理论提出,那些长度短且功能异常的端粒,无法借助现有已知的DNA修复机制得到修复。因此会引发持续的 DNA 损伤反应,从而造成细胞衰老。
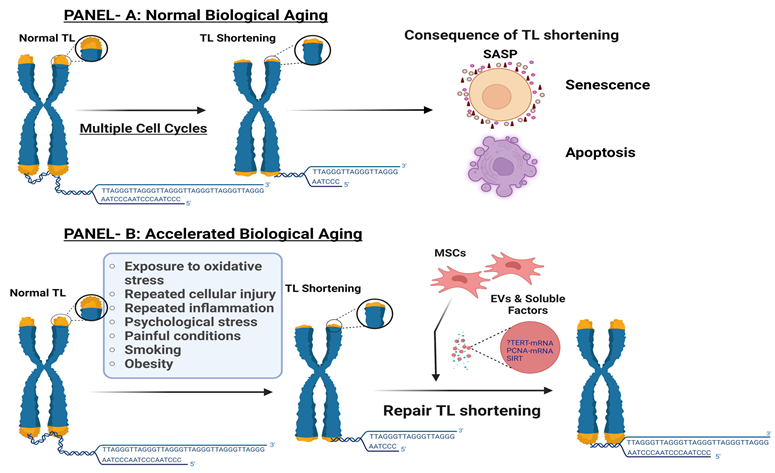
间充质干细胞(MSCs)在预防端粒缩短和细胞衰老过程中发挥着关键调控作用。它们通过多个靶点的协同效应延缓衰老发展,主要作用机制涵盖:激活端粒酶并维持端粒完整性、抑制氧化应激与炎症反应、修复干细胞微环境、调控衰老相关通路。
举例来说,端粒酶作为调节端粒长度的 “分子修复装置”,能通过添加 TTAGGG 序列来抵消端粒在复制过程中的缩短,进而维持染色体稳定性。在抗衰老研究领域,提高端粒酶活性被认为是延缓细胞衰老的重要手段。
此外,MSCs 分泌的细胞外囊泡(EVs,例如外泌体)能够携带 hTERT 蛋白(即端粒酶逆转录酶)和 PCNA mRNA(参与端粒修复),当它们转移到受体细胞后,会激活端粒酶活性,从而维持端粒长度。
围产组织来源干细胞:抗衰老的 “优等生”
值得关注的是,干细胞的抗衰老效果并非 “千篇一律”,其中围产组织(胎盘、脐带、羊膜等)来源的 MSCs 表现尤为突出,其效果显著优于骨髓、脂肪等成体组织来源的 MSCs。
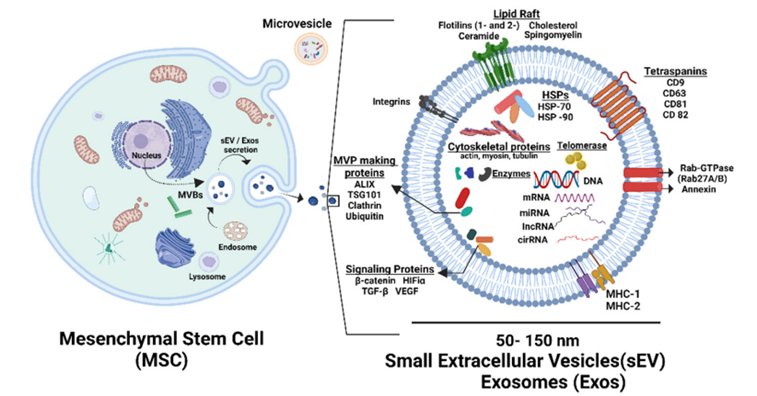
这背后的核心优势可归结为四点:
1. 端粒 “先天优势” 更突出
围产组织来源的MSCs 的端粒长度天生更长:
脐带 MSCs 的端粒比骨髓 MSCs 长 30%-50%,且培养过程中缩短速度更慢;
胎盘来源的 MSCs 端粒长度甚至接近胚胎干细胞,维持能力更强。
同时,围产组织来源的MSCs 能持续表达 hTERT(端粒酶逆转录酶),而骨髓 MSCs 端粒酶活性极低,只能依赖缓慢的替代途径维持端粒,效率大不如前。
2. 增殖能力强,衰老来得更晚
胎源 MSCs 的 “生长效率” 更高:
胎源MSCs的群体倍增时间(PDT)更短(如脐带MSCs:24–48小时vs. 骨髓MSCs:48–72小时),可传代20–40代仍保持未衰老状态,而骨髓MSCs通常在 10–15代进入衰老期。
而胎源MSCs的SA-β-gal阳性细胞比例(衰老标志物)显著低于成体MSCs,且SASP因子(如IL-6、MMPs)分泌量更低。
3. 免疫兼容好,抗炎能力更优
在安全性上,围产 MSCs 几乎不表达引发移植排斥的 HLA-DR 分子,还能分泌 IDO、PGE2 等 “免疫调节剂”,抑制 T 细胞过度活化,降低排斥风险。
抗炎方面,脐带 MSCs 外泌体携带的 miR-146a、miR-21 等分子,能精准靶向炎症信号,有效减轻组织氧化应激损伤。
4. 高效修复,旁分泌效应更强
围产 MSCs 分泌的 HGF、VEGF、IGF-1 等生长因子浓度远高于骨髓 MSCs,能更高效促进组织修复和干细胞微环境再生。
胎源MSCs-EVs携带 hTERT蛋白、PCNA mRNA、端粒DNA片段,可直接转移至受体细胞,延长端粒并减少衰老,例如:脐带MSCs-EVs通过递送PCNA mRNA,激活骨髓MSCs的ALT途径,使其端粒长度增加 20–30%。
结语
间充质干细胞及其分泌物正在为人类对抗衰老提供越来越清晰的路径。围产组织来源的 MSCs 凭借更优的端粒维持能力、更强的增殖活性与免疫兼容性,成为抗衰老研究中极具潜力的 “种子选手”。
随着科学对细胞衰老机制的探索不断深入,这些藏在生命早期组织中的 “年轻力量”,不仅让我们更懂衰老的本质,更在延缓衰老、守护健康的道路上点亮了新的希望。或许在不久的将来,依托这些前沿研究,“让衰老来得更慢、更健康” 将从科学愿景逐步照进现实,为生命质量的提升注入持久动力。
参考文献:
[1]Arellano, M. Y. G. et al. Role of Mesenchymal Stem/Stromal Cells (MSCs) and MSC-Derived Extracellular Vesicles (EVs) in Prevention of Telomere Length Shortening, Cellular Senescence, and Accelerated Biological Aging. Bioengineering 11, 524 (2024).
[2]Lei, Q. et al. Extracellular vesicles deposit PCNA to rejuvenate aged bonemarrow-derived mesenchymal stem cells and slow age-related degeneration. SciTransl. Med.13, eaaz8697 (2021)
[3]Oh, M., Lee, j., Kim, Y. J., Rhee, W. J.& Park, J. H. Exosomes Derived fromHuman Induced Pluripotent Stem Cells Ameliorate the Aging of Skin Fibroblasts. int.J. Mol. Sci. 19, 1715 (2018).
内容来源网络公开资料,锐赛新媒体中心 综合整理。
声明:本文内容仅用于科普交流,不构成任何医疗建议或治疗方案推荐。
文中涉及的科研成果、临床数据等信息均来源于公开文献及权威机构发布,仅供参考。由于医学的复杂性,个体案例不代表普遍疗效,请勿盲目解读。
本平台不对用户基于本文内容作出的任何决策承担责任,相关治疗请务必前往正规医疗机构,在专业医生指导下进行。
本文图片来源网络,如有版权问题请联系删除。本声明最终解释权归公众号所有。


